
Diagnose einer Akuten Myeloischen Leukämie
Vom Hausarzt überwiesen worden wegen dem Verdacht auf eine akute myeloische Leukämie. Wie wird diese eigentlich diagnostiziert? Das klären wir in diesem Film mit Herrn Professor Aulitzky vom Robert-Bosch-Krankenhaus in Stuttgart.
Keine Lust zu lesen? Hier sind alternative Medien:
Sie sehen gerade einen Platzhalterinhalt von Standard. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf den Button unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Weitere InformationenDie erste Auffälligkeit ist meistens ein pathologisches Blutbild. Dieses wird mit bestimmten Verfahren analysiert, die Zusatzinformationen geben. Damit kann man meistens relativ präzise Diagnosen wie akute Leukämie, akute lymphatische oder akute myeloische Leukämie stellen. Der nächste Schritt ist eine Knochenmarksuntersuchung. Für diese sind die Vorergebnisse wichtig, weil man damit die tiefergehenden Untersuchungen aus dem Knochenmark weiter steuern kann.
Knochenmarkuntersuchung
Bei der Knochenmarkuntersuchung wird am Beckenkamm untersucht. Das hat mit dem Rückenmark nichts zu tun. Die Knochenmarkuntersuchung ist eine relativ wenig belastende Untersuchung, die man aus diesem Grund auch bei katastrophalen Blutwerten umgehend durchführen kann, da man sie in lokaler Betäubung durchführt. Eine Operation wäre zum Beispiel bei schlechten Blutwerten schwierig. Aus dem Knochenmark werden Knochenmarkbröckchen herausholt und einer Untersuchung zugänglich gemacht. Dort entsteht das Blut und dort ist auch die Ursache der Erkrankung. Deshalb muss man dort nachschauen. Hier sieht man erstens die Blutbildung bzw. ob die Blutbildung noch in Resten vorhanden ist und zweitens sieht man die Art der Leukämie. Drittens gewinnt man in diesen Bröckchen auch teilungsfähige Zellen, die z. B. die Untersuchung der Chromosomen möglich macht. Daher hat man mit der Knochenmarkuntersuchung praktisch alle Informationen über die Art der Erkrankung, die vorliegt.
Allgemeiner Gesundheitszustand
Bevor man weiter diagnostiziert, wird der allgemeine Gesundheitszustand untersucht. Die anstehenden Therapien sind sehr belastendend. Deshalb ist es wichtig zu wissen, wie fit ein Patient ist. Dazu gehört auch, dass man weiß, welche Organe Begleiterkrankungen haben und welche Organe Vorschäden haben, damit die Belastbarkeit dieses Menschen gut eingeschätzt werden kann. Daher gehört immer eine allgemeine internistische Untersuchung dazu, bei der man weiß, ob Herz und Leber gesund sind oder ob es Einschränkungen gibt, die man bei der Wahl der Medikamente berücksichtigen muss.
Ausbreitungsdiagnostik
Blut ist überall, das heißt eine Leukämie ist nicht durch eine Operation der Nasenspitze heilbar. Es handelt sich um eine Ausbreitung im ganzen Körper. Neben der Ausbreitung im Blutbild in den Organen gibt es in seltenen Fällen auch Ausbreitungen, die andere Maßnahmen notwendig machen. Dazu gehört zum Beispiel der Befall der Gehirnhäute, weil manche Medikamente nicht gut in den Nervensystemraum eindringen können. Dann muss man spezielle Medikamente wählen oder den Rückenmarksraum speziell behandeln. Andere Formen, die spezielle Maßnahmen benötigen, sind seltenen Varianten, bei denen irgendwo Knoten entstehen. Leukämien können also auch manchmal zu Knotenbildung neigen und das führt dazu, dass man zum Beispiel eine Region zusätzlich bestrahlen muss. Daher gehört trotz dieser allgemeinen Ausbreitung der Leukämien eine Ausbreitungsdiagnostik dazu, um ein präzises Gesamtbild der Erkrankung zu bekommen.
Typische Marker bei der AML
Die Zellen haben teilweise Marker auf der Oberfläche, wie Proteine, mit denen sie mit ihrem Umfeld kommunizieren. An denen kann man teilweise erkennen, welche Krankheit diese Zelle hat.
Welche Marker sind in dem Fall typisch?
Bei der akuten myeloischen Leukämie können wir einerseits mit Markern feststellen, ob es eher eine Zelle ist, die von Monozyten oder von Granulozyten abstammt. Da spielen Marker wie zum Beispiel CT 14 eine Rolle. Aber wichtiger sind Marker, die beweisen, dass es sich dabei um eine sehr unreife Zelle handelt, die in ihrem Reifungsprozess steckengeblieben ist. Und hier spielen Marker wie CD34 oder CD117 eine Rolle. Und zusätzlich ist der Nachweis dieser Marker wie zum Beispiel CD117 erforderlich, um sicher sagen zu können, dass es sich nicht um eine lymphatische Leukämie handelt.
Die Zellen sind teilweise dermaßen plastisch, dass man diese nicht mehr richtig unterscheiden kann, da sie alle gleich aussehen.
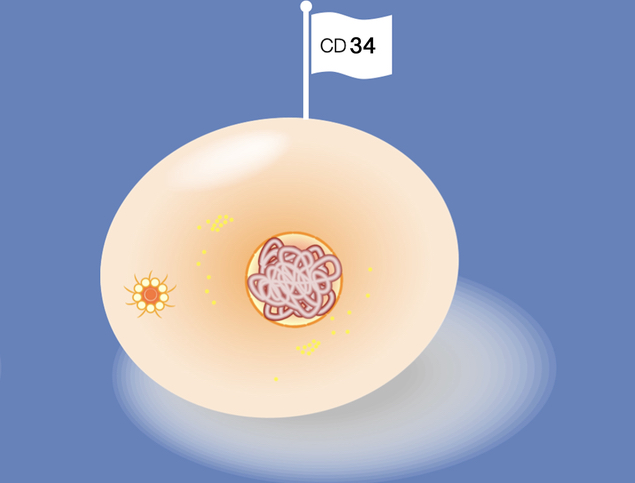
Unreife Zellen – Blasten
Ein Blast ist eine unreife Zelle. Gesunde Menschen haben auch Blasten im Knochenmark, aber sie dürfen eine bestimmte Häufigkeit nicht überschreiten. Sind mehr als 5% Blasten im Knochenmark, ist es nicht mehr normal. Sind mehr als 20% Blasten im Knochenmark, kann die Diagnose einer akuten Leukämie gestellt werden.
Chromosomentranslokation
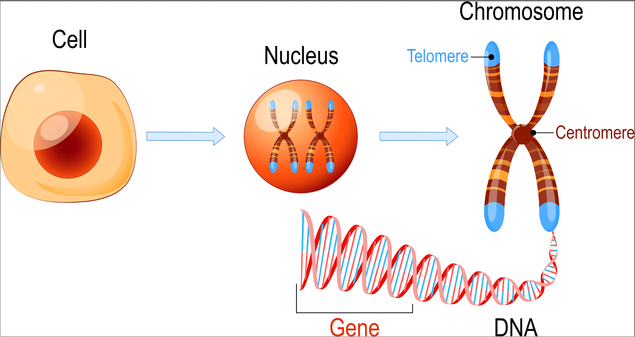
Schaut man noch detaillierter in die Zelle, sind dort die Chromosomen, auf denen die Informationen der Zelle gelagert sind. Auf den Genen passieren oftmals Fehler. Die Zelle vervielfältigt sich und es werden irgendwelche Schreibfehler gemacht. Man spricht hier von Chromosomentranslokation oder dass Dinge gelöscht oder dupliziert werden. Bei Chromosomenveränderungen und Veränderungen, die so klein sind, dass sie sich im Gesamtchromoson nicht zeigen würde, spricht man von Mutationen.
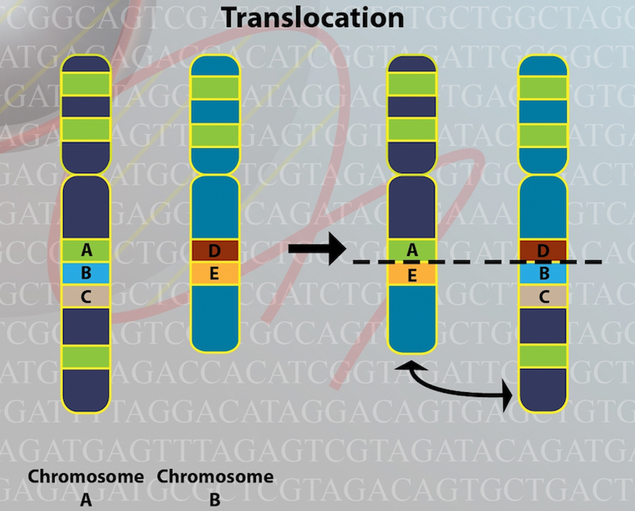
Chromosomale Veränderungen gibt es überall dort, wo sich Chromosomen falsch zusammenfügen. Fügen sich Anteile verschiedener Chromosomen falsch zusammen, nennt man das Translokationen.
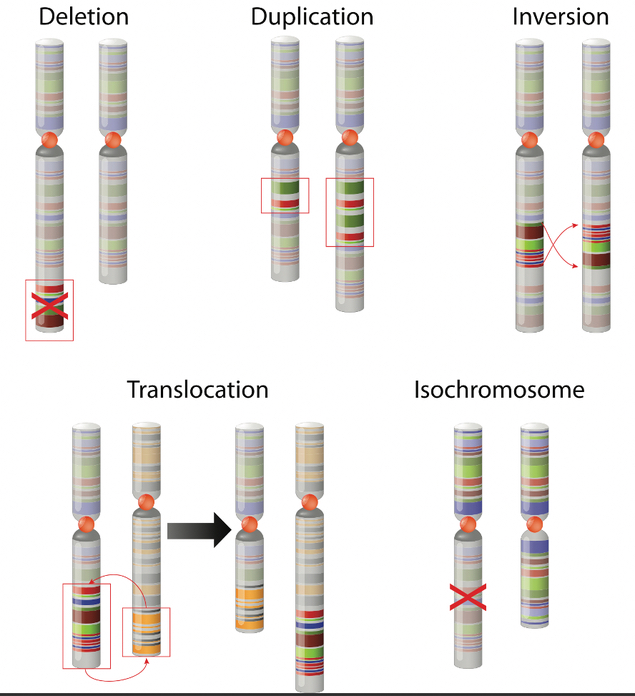
Es können Stücke verlorengehen oder gewonnen werden. Im Endeffekt führen diese Veränderungen immer dazu, dass Funktionen bestimmter Eiweißmoleküle nicht mehr vorhanden oder überschüssig vorhanden sind. Das ist der Schritt, der letztlich dazu führt, dass eine Zelle von einer gutartigen zu einer bösartigen wird.
Translokation noch einmal anschauliche erklärt: Chromosom 1 hat die Nachricht, die Ampel ist grün und deshalb darf ich fahren. Das Chromosom 2 hat die Nachricht, die Ampel ist rot und deshalb muss ich stehen. Wenn ich jetzt eine Translocation habe (wenn die Enden von diesen beiden Chromosomen vertauscht werden), dann kommt am Ende die Nachricht: Die Ampel ist grün und deshalb muss ich stoppen und die Ampel ist rot und deshalb darf ich fahren. Man sieht direkt, dass das gefährlich ist.
Die Gene sind chemische Buchstabenketten, die einen Sinn haben. Durch diese Translokationen wird der Sinn oder die Funktion dieses Proteins alteriert. Es können Wachstumssignale, die normalerweise reguliert stattfinden, plötzlich völlig irregulär aktiv bleiben und auf die Art und Weise das Wachstum der Zellen endlos stimulieren. Auch das Gegenteil gibt es: Signale können gestört sein, die normalerweise dazu beitragen, dass sich die Zelle zu ihrer Endzelle entwickelt, und deshalb bleibt sie stecken. Exakt solche Veränderungen werden durch die Translokationen verursacht.
Typische Mutationen für die AML
Die Gut-Risiko AMLs sind alle durch große chromosomale Veränderungen charakterisiert, die ganz typisch sind und die auch für diese Formen von Leukämien eindeutig sind. Das sind Veränderungen, bei denen hauptsächlich Translokationen zugrunde liegen und die dazu führen, dass die Ausreifung dieser Zellen steckenbleibt.
Daneben gibt es Veränderungen, die man auch bei anderen bösartigen Erkrankungen findet. Wie zum Beispiel Mutationen in einem Gen, das P53 heißt. Das sind Veränderungen, die eine sehr problematische Prognose anzeigen und die eine Heilungschance bei diesem Patienten nur mit Transplantation erhoffen lassen.
Zum dritten gibt es Veränderungen, die gleichzeitig als Zielstruktur für Medikamente dienen, und die damit zusätzliche therapeutische Möglichkeiten durch moderne, zielgerichtete Therapieformen ermöglichen.
Zielgerichtet in welchem Sinne? Sind das Antigene oder Inhibitoren?
Das sind zielgerichtete Inhibitoren wie zum Beispiel Inhibitoren für das FLT3 Gen, die allein auch schon in der Lage sind, zumindest vorübergehend komplette Rückbildungen zu erreichen.
HLA
Im Rahmen der Diagnose akuter Leukämien gibt es noch eine weitere Untersuchung, die eventuell notwendig ist. Das ist die HLA Typisierung. HLA heißt „Human leucocyte antigen“. Das sind Gewebsverträglichkeitsmerkmale. Merkmale, die bestimmen, ob ein Transplantat zusammenpasst oder nicht.
Diese Bestimmung ist essenziell bei zwei Gruppen von Menschen. Bei all denen, wo eine Transplantation in Frage kommt, weil man mit dieser Information nach einem Spender suchen kann. Zum zweiten entwickeln manche Patienten viele Antikörper gegen fremde HLA Moleküle. Das sind ganz typisch Mütter von Kindern, weil sie gegen das fremde HLA ihres Kindes Antikörper produzieren. Und diese kann man schwer mit Thrombozyten ersetzen. Auch hierfür braucht man die HLA Typisierung, um passende Thrombozyten-Präparate zu bekommen.
Drei unterschiedliche Gruppen bei der Risikobewertungen
Es gibt Erkrankungen, bei denen die Heilungsrate mit konventioneller Chemotherapie in der Größenordnung von 70/80% liegt. Diese Gruppe bezeichnen wir als Gut-Risiko, weil wir uns gut drauf verlassen können, dass die Menschen geheilt werden, ohne dass man eine Transplantation durchführt.
Eine zweite Gruppe heilt man ohne Transplantation nie. Diese Patienten werden als Hoch-Risiko bezeichnet und benötigen für das Heilungsziel eine Transplantation.
Und dann gibt es eine dritte Gruppe, die zwischen den beiden liegt. Bei perfektem Ansprechen kann man von einer Heilung ausgehen und bei suboptimalem Ansprechen ist das Rezidiv-Risiko relativ hoch ist. Hier muss aus dem Verlauf entschieden werden, ob eine Stammzell-Transplantation zusätzlich erforderlich ist.

